《港湾商业观察》萧秀妮
2026年2月3日,专注于细菌感染及细菌代谢相关疾病领域的生物科技公司丹诺医药(苏州)有限公司(以下简称,丹诺医药)向港交所递交招股书,拟在主板上市,中信证券与农银国际担任联合保荐人。
作为一家临近商业化阶段的创新药企,丹诺医药已构建起涵盖7款候选药物的差异化管线,其中核心产品利福特尼唑已完成Ⅲ期临床试验并筹备新药上市申请(NDA),有望成为全球首款针对幽门螺杆菌感染的新分子实体药物。然而,公司尚未实现产品商业化及收入突破,报告期内持续亏损且依赖外部融资,商业化进程中的多重风险亦不容忽视。
1
三款独家创新药瞄准未满足临床需求
据天眼查显示,丹诺医药成立于2013年,核心业务聚焦细菌感染及细菌代谢相关疾病的创新药研发,目前已建立起由7项创新资产组成的产品管线,涵盖临近商业化、后期临床、IND批准及临床前多个阶段,其中三款核心/主要产品均为全球首创的创新型候选药物,针对未被满足的临床需求,现有竞争主要来自传统超适应症疗法或同领域传统药物,无直接同机制创新药竞争。
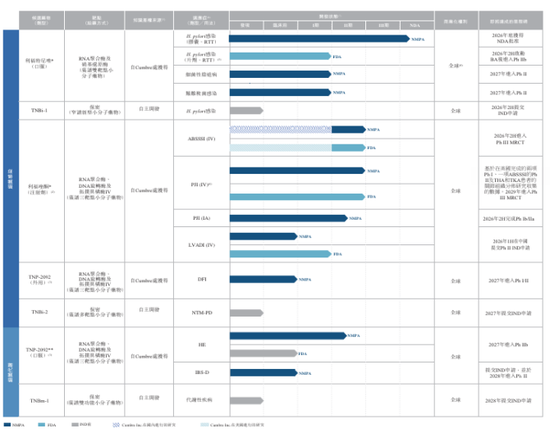
作为公司进度最快的核心产品,利福特尼唑(TNP-2198)是自1982年幽门螺杆菌被发现以来,全球首款且唯一接近商业化的针对该细菌感染的新分子实体候选药物。其通过利福霉素与硝基咪唑两个药效团偶联形成,可同时抑制细菌RNA聚合酶及硝基还原酶,通过双靶点协同机制发挥杀菌作用,对微需氧菌和厌氧菌均有效,能有效克服抗菌药耐药性这一全球性难题。
招股书显示,该产品已完成RTT对比BQT的中国Ⅲ期头对头临床试验,结果显示其根除率超90%,在多重耐药人群中表现出显著优效性,且安全性与耐受性优于现有一线疗法铋剂四联疗法(BQT)。不仅如此,该产品无需提前进行药敏试验,可与尿素呼气试验(U *** )无缝衔接,且给药便捷,患者依从性优势显著。
目前,利福特尼唑已向国家药监局提交NDA并获得受理,预计2026年底获批;同时,其在美国已获得IND许可、快速通道及合格抗感染产品(QIDP)认定,有望受益于FDA加速审评流程。除幽门螺杆菌感染外,公司还计划推进其治疗细菌性 *** 病及艰难梭菌感染的临床开发。
从市场空间来看,幽门螺杆菌感染已成为重大公共卫生挑战,世界卫生组织已将其列为I类致癌物,约80%的胃癌与该细菌感染相关。根据弗若斯特沙利文数据,2024年中国幽门螺杆菌感染人数达6.211亿,全球感染人数更是高达40.810亿。
而现有治疗方案面临严重的耐药性问题,丹诺医药Ⅲ期临床试验数据显示,初治患者中,幽门螺杆菌对克拉霉素、甲硝唑、左氧氟沙星的耐药率分别达40.8%、68.2%、35.1%,对至少一种指南推荐抗菌药的耐药率高达85.1%,多重耐药率达46.3%,这为利福特尼唑提供了广阔的市场替代空间。
利福喹酮(TNP-2092 注射剂)是全球首创的三靶点抗菌候选药物,通过利福霉素与喹嗪酮药效团偶联形成,可同时抑制细菌RNA聚合酶、DNA旋转酶和拓扑异构酶Ⅳ,在临床可实现剂量下有望对生物膜感染有效,专门针对人工关节感染(PJI)、急性细菌性皮肤和皮肤结构感染(ABSSSI)等植入体相关细菌感染的治疗。
招股书显示,利福喹酮注射剂已获得国家药品监督管理局和FDA的IND批准,用于治疗人工关节感染(PJI)和急性细菌性皮肤及皮肤结构感染(ABSSSI),并且已在中国和美国完成六项临床试验,包括两项I期临床试验、三项临床药理学试验及一项Ⅱ期临床试验。在美国开展的Ⅱ期临床试验中,利福喹酮治疗ABSSSI的疗效优于常用抗生素万古霉素,在mITT人群的早期临床反应率达76.9%,高于万古霉素组的67.5%;尤其在耐药菌株感染中优势更为显著,对甲氧西林耐药金黄色葡萄球菌(MRSA)的早期临床反应率达78.1%(万古霉素组57.9%),对喹诺酮耐药金黄色葡萄球菌(QRSA)的反应率达75.9%(万古霉素组55.6%)。
此外,针对全髋/膝关节置换术患者的关节组织分布研究显示,利福喹酮在滑液及骨组织中能达到高浓度,预计超过针对90%的PJI临床分离株的更低生物膜杀菌浓度(MBBC₉₀),具备无需手术即可控制感染的潜力。
植入体相关细菌感染市场需求迫切,受医疗技术进步及人口老龄化推动,植入医疗器械使用日益普遍,但传统抗生素难以穿透细菌生物膜,治疗效果有限。根据弗若斯特沙利文数据,全球PJI发病率预计将由2024年的8.64万例增至2035年的42.58万例,2024-2029年复合年增长率13.8%,2029-2035年达17.1%;中国PJI发病率预计由2024年的2.25万例增至2035年的8.65万例,复合年增长率11.7%。截至最后实际可行日期,全球尚无用于治疗PJI的创新型抗菌药物获批,利福喹酮作为唯一处于临床开发阶段的小分子候选药物,具备显著的先发优势。
主要产品TNP-2092口服制剂是全球首个用于治疗肠道菌群代谢相关疾病的多靶点抗菌候选药物,针对肝性脑病(HE)和腹泻型肠易激综合征(IBS-D)等适应症。其作用机制与利福昔明类似(肠道局部作用且全身暴露量极低),但对肠道产氨细菌的活性更优,且对益生菌的选择性更高,自发耐药频率极低。
临床数据显示,TNP-2092口服制剂在降低血氨方面效果优于利福昔明,而高氨血症是HE发展的关键诱因,这使其在HE治疗中具备显著竞争力。目前,该产品已在中国完成四项I期及Ⅱ期临床试验,概念验证数据已验证其疗效及安全性。
从市场规模来看,2024年中国肝性脑病患病率达170万例,全球达930万例;中国腹泻型肠易激综合征患者达1.199亿例,全球达4.897亿例。利福昔明作为当前临床常用药物,2024年全球销售额达20亿美元,但该药物在中国大陆尚未获批用于HE或IBS-D治疗,且存在耐药频率较高的问题,TNP-2092口服制剂有望凭借更优的疗效和安全性实现市场替代。
除上述三款核心/主要产品外,丹诺医药的管线还包括TNP-2092外用制剂、TNBi-1新型小分子药物、TNBi-2多靶点偶联药物、TNBm-1双功能小分子药物。
其中TNP-2092外用制剂主要针对糖尿病足感染,对MRSA、QRSA等耐药菌株及生物膜相关感染具有强杀菌活性,已获中国IND批准,预计2027年启动I/Ⅱ期临床试验。
TNBi-1新型小分子药物则是通过靶向幽门螺杆菌电子传递链削弱ATP合成,对肠道菌群无活性,目前处于先导化合物优化阶段,预计2026年提交IND申请。
TNBi-2多靶点偶联药物主要针对非结核分枝杆菌肺病(NTM-PD),有望简化治疗方案、降低耐药率,处于先导化合物优化阶段,预计2027年提交IND申请。
TNBm-1双功能小分子药物,靶向肠道细菌代谢通路及宿主核受体,用于代谢性疾病治疗,处于先导化合物识别阶段,预计2028年提交IND申请。
2
持续亏损研发投入下降,经营现金流为负
尽管管线布局亮点突出,但丹诺医药目前尚未有产品获批商业化,未产生任何产品销售收入,报告期内持续录得净亏损。2023年、2024年及2025年前9月(报告期内),公司净亏损分别为1.92亿元、1.46亿元及1.16亿元,主要因研发开支高企及行政开支增加所致。
公司报告期内还获得一定规模 *** 补助,2023年、2024年及2025年前9月分别确认 *** 补助444.4万元、493.8万元、118.1万元,同时通过结构性存款等金融资产获得少量公允价值收益及银行存款利息收入。
值得注意的是,丹诺医药供应商集中度高,依赖第三方生产。报告期内,公司对前五大供应商的采购金额分别为4165.5万元、3299.2万元、1076.7万元,占年度采购额的比例分别达49.5%、80.8%、70%。
报告期内,更大供应商依次是一家总部位于中国上海的CRO服务公司;一家总部位于中国重庆、在深圳证券交易所上市提供CDMO服务的公司;一家全球性的CRDMO(合同研发及制造组织),在上海证券交易所及香港联交所上市,业务横跨亚洲、欧洲及北美。向更大的供应商采购额分别为1732.1万元、1790万元、628.3万元,占年度采购额的比例分别为20.6%、43.8%及40.8%。
此外,公司依赖第三方生产临床及商业化所需药品,若第三方生产设施未能通过监管批准,或生产过程中出现质量问题,也将对业务产生重大不利影响。
生产方面,公司目前无自有生产设施,临床阶段及未来商业化初期均依赖CDMO合作生产;自有cGMP标准生产设施预计2028年才投入运营,若第三方未能按要求提供足够数量、合格质量或合理价格的药品,将影响商业化进程。
对此,资深财经评论员郭施亮表示,商业化初期比较单一的供应链体系可能会影响自身竞争力,轻资产模式关键要保障后续现金流供应以及后续风险管理能力,一旦供应链过度依赖某一公司,或商业化受阻,会对公司后续发展产生一定的影响压力。
创新药企的研发属性决定其面临高风险。研发层面,尽管核心产品进度领先,但临床开发结果存在不确定性,且专利保护面临挑战——截至最后实际可行日期,公司已有14项物质组成专利到期,1项将于2028年到期,虽通过用途、制剂等专利补充保护,但仍可能面临仿制药竞争。
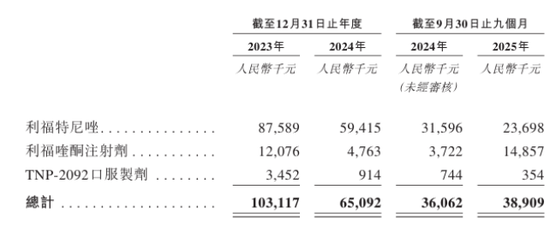
研发投入方面,丹诺医药金额呈现下降趋势。报告期内,其研发开支分别为1.08亿元、6983.8万元、4639.5万元,占各期经营开支总额的比例分别达84.8%、84.2%、56.2%。其中核心产品利福特尼唑和利福喹酮注射剂为研发投入重点,合计占研发开支总额的比例分别为91.9%、91.9%、83.1%,凸显公司对核心管线商业化的聚焦。
财务结构方面,2023年及2024年,公司录得负债总额分别为8.55亿元、10.31亿元,资产总值分别为9605.4万元、1.33亿元,资产负债率高达890.09%、775.8%;而截至2025年9月30日,公司负债总额为8824.2万元,资产总额为2.66亿元,资产负债率大幅降至33.21%,主要因赎回负债终止确认及E2、E3轮融资带来现金流入。
现金流方面,丹诺医药报告期内经营活动现金流净额持续为负,分别为-9811.6万元、-4860.1万元、-6945.1万元;融资活动现金流净额则持续净流入,分别为472.6万元、8849.7万元、1.91亿元。截至2025年前三季度,公司期末现金及现金等价物增至2.22亿元,为后续研发及商业化提供资金支撑。
3
商业化布局绑定远大生命科学,近8亿合作背后暗藏“对赌”
招股书显示,为推进核心产品商业化,丹诺医药已与远大生命科学订立独家商业化合作协议,就利福特尼唑在大中华区(不包括台湾)的营销、推广及分销达成合作。
根据协议,远大生命科学将支付更高不超过7.75亿元的款项,具体包括2500万元独家前期费用、两期里程碑付款及销售梯度里程碑付款,丹诺医药则需支付相应推广服务费率,且从初始75%逐步降至65%。
同时,后续还有多轮里程碑式的付款。具体而言,一是商业化里程碑付款,两期合计6500万元,分别于利福特尼唑首个适应症获得中国上市许可、纳入国家医保药品目录时触发;二是推广里程碑付款更高7100万元,分六期支付,按累计年度净销售额门槛触发。除此之外,还有推广奖励付款,更高2000万元,首次达到指定年度销售净额门槛后分两期支付。
然而,该合作存在明确的业绩约束条款:若丹诺医药未能于2026年12月31日前获得利福特尼唑首个适应症的中国上市许可,远大生命科学可单方面终止协议,公司需退还已收首期里程碑付款;若该产品未被纳入2027年版国家医保药品目录,合作方有权要求重新协商商业条款,协商未果则协议可能终止。
郭施亮表示,严格业绩约束是一把双刃剑,提前锁定未来现金流,并且未来有机会做大做强公司商业体系,有利于相关产品的加快上市。不利因素,可能会影响公司长期议价能力,长期不确定性仍在增加。在公司产品销量尚未形成规模化增长之前,成本控制压力大,议价能力比较弱。
除合作风险外,丹诺医药商业化还面临多重挑战。首先是销售与分销能力不足,公司自成立以来主要聚焦研发,尚未建立自身的销售与营销团队,缺乏商业化经验,高度依赖远大生命科学的销售 *** 。公司于招股书中进行风险提示,若未来计划全球分销,还需投入大量资源建设内部营销组织及销售团队,面临与成熟药企的人才竞争。
市场认可方面,现有细菌控制疗法已获得医学界广泛采用,医生、患者及第三方支付方对新产品的接受度存在不确定性;且专业协会、 *** 机构等发布的相关指南或研究可能对产品使用产生不利影响。
医保准入方面,药品定价受 *** 监管,能否纳入国家医保药品目录将直接影响市场渗透率;即使纳入医保,也可能面临大幅降价压力,影响盈利空间。
合规与运营层面,公司存在租赁协议未完成登记的合规瑕疵,虽预计罚款金额不大,但可能面临行政监管风险;同时,药品研发过程中收集的数据准确性、生产设施监管批准、知识产权保护等均可能对业务产生重大影响。此外,公司自成立以来持续亏损,未来若无法通过产品销售实现盈利,将面临持续的资金压力。
自成立以来,丹诺医药已完成7轮融资,投资方包括北极光创投、原点创投、高特佳投资等知名机构,最后一轮融资投后估值为20.13亿元,为公司管线研发及商业化筹备提供了重要资金支持。
股权结构方面,截至最后实际可行日期,Cumbre实体为丹诺医药的单一更大股东集团,可行使约18.82%的投票权,该集团为被动财务投资者,不参与公司日常营运。公司创始人、董事长兼CEO马振坤博士连同ESOP平台控制约13.61%的投票权,其在传染病领域新药开发拥有超过30年经验,为公司核心管理力量。(港湾财经出品)
